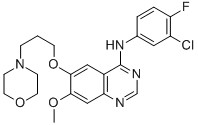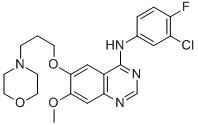
Tratamento contra o câncer de 91371 células do pulmão dos esteroides AKOS dos Peptides de Gefitinib 184475-35-2
-
Realçar
pó do enanthate do methenolone
,pó do propionate da testosterona
-
Lugar de origemChina
-
MarcaRUN
-
CertificaçãoISO9001
-
Número do modeloRUN-AH
-
Quantidade de ordem mínima10g
-
Preçoinquiry
-
Detalhes da embalagem10g 50g 100g 500g 1kg
-
Tempo de entrega3-7 dias
-
Termos de pagamentoT/T, MoneyGram, BTCcoin
-
Habilidade da fonte1kg --100kg
Tratamento contra o câncer de 91371 células do pulmão dos esteroides AKOS dos Peptides de Gefitinib 184475-35-2
Tratamento contra o câncer de 91371 células do pulmão dos esteroides AKOS dos Peptides de Gefitinib 184475-35-2
| Indicações e usos | Gefitinib é uma droga antineoplástica da terapia do alvo com especificidade relativamente alta que foi desenvolvida pela companhia farmacéutica britânica AstraZeneca; é a primeira droga visada molecular a ser usada no tratamento contra o câncer não-pequeno do pulmão da pilha. Os fatores de crescimento epidérmicos (EGF) são um tipo do polipeptídeo com uma massa molecular relativa de 6.45x103, e podem ligar com os receptors epidérmicos (EGFR) do fator de crescimento em superfícies da membrana de pilha do alvo para provocar efeitos biológicos. EGFR é um tipo de tipo receptor de (TK) da quinase da tirosina, assim que quando encadernado com EGF, promoverá a ativação do TK no receptor. Isto causará o resíduo da tirosina no receptor ao autophosphorylate e enviará sinais divisores contínuos na pilha, causando a proliferação de pilha e a diferenciação. EGFR é abundante no tecido humano, e é expressado altamente em tumores caluniados. Gefitinib obstrui o caminho da transdução do sinal da superfície EGFR da pilha para impedir o crescimento, a metástase, e o crescimento do tumor em vasos sanguíneos, e pode induzir o apoptosis da pilha do tumor. Gefitinib é usado principalmente para tratar o câncer pulmonar da pilha da não-haste. |
| Farmacocinética | É oralmente eficaz, com absorção e metabolismo relativamente lentos depois da entrada. A disponibilidade biológica de uma única dose 250mg oral é quase 60%, e sua área sob a curva (AUC) é dependente da dosagem. Com únicas dosagens diárias, a concentração do sangue é constante após 7-10 dias, com a concentração do sangue que repica 3-7 horas após a medicamentação e então gradualmente depois da redução bifásica (sua meia-vida é 12-58 horas, em uma média de 28 horas). Observa-se como farmacocinética dependente da dose, e depois das dosagens múltiplas, do AUC e do Cmax aumentados proporcionalmente. Quando tomado com alimento, seus Cmax e AUC não diminuíram significativamente. Sua taxa obrigatória da proteína do plasma é quase 90%. Gefitinib é metabolizado com muitos caminhos diferentes nos fígados em um processo relativamente complicado; o componente principal de seu metabolismo oxidativo é a enzima CYP3A4 do citocromo P450, que metaboliza principalmente metabolitos de O-Desmethyl. Os metabolitos são não relacionados aos efeitos farmacológicos da droga original. A droga original e muitos metabolitos estão passados na maior parte através do intervalo biliar e excretados através da fezes, quando a quantidade de droga excretada através da urina for menos de 4% a quantidade original da dosagem. |
| Reações adversas | Gefitinib bem-é tolerado relativamente, e a maioria de reações negativas são suaves e reversíveis, as características que são vastamente diferentes daquelas de reações negativas padrão às drogas citotóxicos. As reações negativas comuns incluem a diarreia, a náusea, os pruridos, a acne, o vômito, e a debilidade. Somente 1% dos pacientes tiveram que cessar o tratamento devido às reações negativas com uma taxa da ocorrência sobre 20%. Igualmente houve uns casos raros da pneumonia intersticial aguda. |
| Avisos e precauções | Gefitinib não é apropriado para pessoal |
| Propriedades químicas | Luz - pó cristalino amarelo |
| Usos | para a pesquisa |
| Usos | Gefitinib é um antineoplástico. |
| Indicações | O gefitinib do inibidor EGFR ou ErbB1 (Iressa (R), AstraZeneca) foi aprovado originalmente pelos E.U. FDA em 2003 sob regulamentos acelerados para o tratamento do câncer pulmonar não-pequeno localmente avançado ou metastático (NSCLC) da pilha após a progressão na quimioterapia do docetaxel- e platina-baseado. AstraZeneca retirou voluntariamente o gefitinib do mercado em 2005, devido à verificação falhada do benefício clínico durante estudos da cargo-aprovação. Em julho de 2015, FDA restabeleceu a aprovação do gefitinib para um grupo diferente dos pacientes (isto é, pacientes de NSCLC com mutações de EGFR). Outros inibidores aprovados da quinase que visam a família de ErbB, que inclui ErbB1/EGFR, ErbB2/receptor epidérmico humano 2 do fator de crescimento (Her2), ErbB3/Her3, e ErbB4/Her4, são erlotinib (Tarceva (R), OSI Pharm.), lapatinib (Tykerb (R), GlaxoSmithKline), vandetanib (Caprelsa (R), AstraZeneca), afatinib (Gilotrif (R), Boehringer Ingelheim), e osimertinib (Tagrisso (R), AstraZeneca). Todos os inibidores aprovados da família de EGFR compartilham de um andaime comum do quinazoline à excecpção do osimertinib, que tem um andaime do pyrimidinylphenylamine que se assemelhe àquele do imatinib e do nilotinib. Gefitinib e o vandetanib adotam o tipo mim modo obrigatório com “DFG-em” e αC-hélice “” na conformação, quando o erlotinib e o lapatinib ligarem “DFG-” com na αC-hélice que adota “para fora” uma conformação. Afatinib e o osimertinib são inibidores covalent com uma parte electrofílica do enone. |
| Marca | 3M |
| Atividade biológica | Inibidor oralmente ativo, seletivo da quinase da tirosina de EGFR (IC 50 = 23-79 nanômetro). Mostra a atividade mínima contra ErbB2, KDR, c-flt, PKC, MEK e ERK-2. O autophosphorylation dos blocos EGFR e inibe o crescimento do tumor nos ratos que carregam uma escala de xenografts humanos. |