461432-26-8 Dapagliflozin S1548 Selleck C21H25ClO6 639-683-0
-
Realçar
461432-26-8 intermediários farmacêuticos
,Intermediários C21H25ClO6 farmacêuticos
,Intermediários farmacêuticos de Dapagliflozin
-
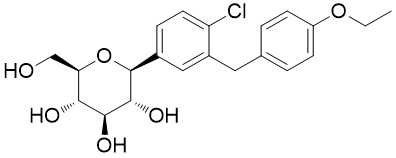
Nome do produtoDapagliflozin
-
SinônimosDAPAGLIFLOZIN; (1S) - [4-chloro-3- [(4-ethoxyphenyl) metílico] phenyl 1,5-Anhydro-1-C-] - D-glucitol
-
CAS461432-26-8
-
MFC21H25ClO6
-
MW408,88
-
EINECS639-683-0
-
Ponto de ebulição°C 609.0±55.0 (previsto)
-
Densidade1,349
-
Pureza99%
-
Lugar de origemChina
-
MarcaRUN
-
CertificaçãoIOS9001
-
Número do modeloRUN-Z
-
Quantidade de ordem mínima10g
-
Preçoinquiry
-
Detalhes da embalagem10g 50g 100g 500g 1kg
-
Tempo de entrega3-7 dias
-
Termos de pagamentoT/T, MoneyGram, BTCcoin
-
Habilidade da fonte1kg --100kg
461432-26-8 Dapagliflozin S1548 Selleck C21H25ClO6 639-683-0
SEÇÃO 1: Informação básica
| Informação básica de Dapagliflozin |
| Interações de droga farmacológicas da segurança do método da síntese das farmacocinética dos efeitos das drogas do diabetes |
| Nome do produto: | Dapagliflozin |
| Sinônimos: | DAPAGLIFLOZIN; (1S) - [4-chloro-3- [(4-ethoxyphenyl) metílico] phenyl 1,5-Anhydro-1-C-] - D-glucitol; Propanediol de Dapagliflozin; BMS-512148-05; Dapagliflozin S1548 Selleck; BASE DE DAPAGLIFLOZIN; Daglican; Dapagliflozi |
| CAS: | 461432-26-8 |
| MF: | C21H25ClO6 |
| MW: | 408,88 |
| EINECS: | 639-683-0 |
| Categorias de produto: | Inibidores; Outros APIs; APIs; Compostos aromáticos; Heterocycles; Intermediários & produtos químicos finos; Fármacos |
| Mol File: | 461432-26-8.mol |
| Propriedades químicas de Dapagliflozin |
| Ponto de ebulição | °C 609.0±55.0 (previsto) |
| densidade | 1,349 |
| pka | 13.23±0.70 (previsto) |
| Informação de segurança |
| Uso e síntese de Dapagliflozin |
| Drogas do diabetes | Dapagliflozin (ForxigaTM) é uma droga anti-diabética nova desenvolvida comummente por Bristol-Myers Squibb e por AstraZeneca, sendo aprovado pela agência de medicinas europeias (EMA) o 12 de novembro de 2012. É igualmente o primeiro inibidor SGLT2 aprovado para o tratamento do tipo diabetes de II, sendo uma opção importante no tratamento do diabetes, e é usado para melhorar o controle glycemic como uma adjunção a dietético e o exercício para adultos com tipo diabetes de II. Dapagliflozin é um inibidor do co-transportador 2 da sódio-glicose. O 8 de janeiro de 2014, os E.U. Food and Drug Administration (FDA) aprovaram-no para ser usada no tratamento do tipo diabetes de II. Entrementes, FDA exige os produtores conduzir a pesquisa do cargo-mercado sobre riscos droga-relacionados. A experimentação do cargo-mercado pedida por FDA inclui uma experimentação cardiovascular do resultado para avaliar o risco cardiovascular para pacientes de alto risco após o tratamento com dapagliflozin na linha de base e em um estudo avaliar o risco de câncer de bexiga em pacientes recrutados. Um outro estudo avaliará o efeito depromoção da bexiga desta droga em animais do roedor. Dois estudos avaliarão as farmacocinética, a eficácia e a segurança do dapagliflozin em pacientes pediatras; um grupo de programa reforçado da farmacovigilância monitorará anomalias do fígado e relatórios do resultado da gravidez nos pacientes que recebem o daglitazone. Dapagliflozin será introduzido no mercado sob o tradename Farxiga pela farmácia de Haoeyou. A informação acima é editada por Andy do chemicalbook. |
| Efeitos farmacológicos | Dapagliflozin trabalha através do transportador de inibição 2 da sódio-glicose (SGLT2), uma proteína no rim que reabsorbs a glicose na circulação sanguínea. Isto permite que a glicose extra seja excretada através da urina, melhorando o controle glycemic sem secreção crescente da insulina. O uso desta droga exige pacientes com função renal normal quando os pacientes de moderado à insuficiência renal severa deverem ser deficientes usar esta droga. A única aplicação desta produto ou combinação com o metformin, o pioglitazone, o glimepiride, a insulina e as outras drogas pode significativamente reduzir o HbA1c e a glicemia de jejum dos pacientes que sofrem o tipo diabetes de II. A frequência da reação adversa era similar ao placebo com o de baixo-risco da hipoglicemia, podendo reduzir o peso corporal. A eficácia do dapagliflozin é comparável com os inibidores do peptidase do dipeptidyl, e diversas drogas hypoglycemic novas, e pode igualmente suavemente abaixar a pressão sanguínea e o peso corporal. A droga tem 5mg e as tabuletas 10mg dois a escolher de, podem tampouco ser usadas apenas ou junto com a insulina, incluindo outras drogas do diabetes. |
| Farmacocinética | Em assuntos saudáveis, o dapagliflozin foi absorvido rapidamente após a administração oral com uma estadia máxima Tmax que é 1 a 2 horas, uma taxa do emperramento da proteína de 91%, uma disponibilidade biológica oral de aproximadamente 78% e uma meia-vida terminal do plasma de 12,9 horas. Após a administração oral, a droga é metabolizada principalmente pelo glucuronosyltransferase 1A9 do diphosphate do uridine (UGT1A9) no metabolito inativo no fígado com a parte menor que está sendo metabolizada pela enzima P450 e de nenhum efeito inibitório ou induzindo na enzima P450. Os protótipos da droga e os metabolitos relacionados foram excretados através da urina (75%) e das fezes (21%). Compare a administração simultânea deste produto com o alimento alto-gordo e com a administração de jejum, Tmax pode ser estendido por 1 dobra, mas a absorção não afetou o grau, assim que pode ser administrada junto com o alimento. As farmacocinética do daglitazone foram afetadas significativamente pela função renal. Os pacientes do diabético com insuficiência renal suave, moderado ou severa são fundidos para ser sujeitos à administração oral de magnésio 20 • daglitazone d-1 por 7 dias. A quantidade sistemática média da exposição, comparada com os pacientes com função renal normal, é respectivamente 32%, 60% e 87% mais altos. Para pacientes com função renal normal, insuficiência suave, insuficiência moderado e insuficiência severa, a quantidade urinária da excreção da glicose em 24 horas de estado estacionário era 85, 52, 18 e 11g, sucessivamente. Kasichayanula e outros estudaram os efeitos farmacocinéticos da deficiência orgânica do fígado no daglitazone. Os pacientes com a insuficiência hepática suave, moderado e severa que tem uma única dose oral de magnésio 10 do daglitazone, o Cmax de cada grupo eram 12% abaixam, 12% mais altos e 40% mais altos do que aquele com função de fígado normal, respectivamente. O AUC de cada grupo era significativamente mais alto do que aquele da função de fígado normal por 3%, por 36% e por 67%. Consequentemente, não se recomenda aplicar o daglitazone aos pacientes da deficiência orgânica renal moderado e severa. Os pacientes severos da deficiência orgânica do fígado precisam de reduzir o uso da dose. |
| Método da síntese | o ácido 5-bromo-2-chlorobenzoic é assunto à cloração acylating, e tem a reação dos Friedel-ofícios com éter phenylethyl para a redução de seu grupo de carbonilo, gerando o metano de 5 bromo-2-chloro-4'-ethoxydiphenyl, sujeitando mais à condensação com 2, 3, 4, 6 acid-1,5-lactone tetra-O-trimethylsilyl-D-GLUCOPYRANOSANOIc. O grupo de hidróxilo anumérico do carbono é sujeito à eterificação e ao deprotection dar 2 chloro-5- (1-methoxy-D-glucopyranose-I-yl) - 4' - ethoxydiphenylmethane, e para usar então Et3SiH/BF3 • OEt2 para que a redução remova methoxy, seguido pela esterificação e pela hidrólise acéticas do anídrido para dar a agentes hypoglycemic o daglitazone com o rendimento total de aproximadamente 40%.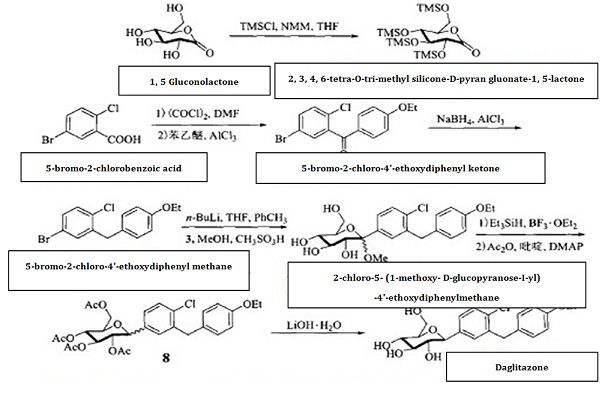 Fig.1 mostra a rota da reação química de sintetizar o dapagliflozin. |
| Segurança | Daglitazone tem a tolerância e a segurança excelentes com a incidência dos eventos adversos associados com o magnésio 10 • daglitazone d-1 que é similar àquele do placebo. Os eventos adversos comuns incluíram a hipoglicemia, o polyuria, a dor nas costas, infecções genitais, infecções de aparelho urinário, dyslipidemia e aumento do hematocrit (HCT). O risco total de hipoglicemia é baixo, e a incidência da hipoglicemia é associada com outros agentes hypoglycemic básicos. A incidência da hipoglicemia era mais alta nos pacientes que sujeitam para articular o tratamento entre o daglitazone e os sulfonylureas ou a insulina comparados com o placebo. Consequentemente, quando este produto é usado em combinação com a insulina ou o secretagogue da insulina, você pode precisar de ajustar a dose da última. |
| Interações de droga | Este produto é metabolizado principalmente no fígado pelo metabolismo UGT1A9, sendo a carcaça da P-glicoproteína. O estudo confirmou que as farmacocinética do daglitazone não estiveram afetadas pelo metformin, o pioglitazone, o sitagliptin, o glimepiride, o voglibose, e o simvastatin, valsartan, o warfarin, e o digoxin. As concentrações do soro das drogas acima mencionadas não são igualmente clinicamente significativamente afetadas pelo daglitazone. Rifampicin pode reduzir a quantidade da exposição de daglitazone por 22% quando o ácido mefenamic puder aumentar a quantidade da exposição do corpo por 51%, mas tem o efeito não clinicamente significativo em 24 excreções da glicose da urina de h. |
| Descrição | A administração terapêutica australiana dos bens (TGA) e a Comissão Europeia aprovaram o dapagliflozin em outubro e novembro de 2012, respectivamente, como uma adjunção para fazer dieta e exercitar para o tratamento do tipo - diabetes 2. Dapagliflozin é uma terapia potencialmente atrativa devido a seu mecanismo glucosesensitive e insulina-independente da ação. É um inibidor SGLT2 seletivo da primeiro-em-classe (IC50=1.1nanômetro; seletividadecontraSGLT1>1000)queabaixaoponto inicialrenalparaareabsorçãodaglicose, permitindo queaglicoseadicionalseja eliminadaatravésdosrins. Emratosnormais, aadministraçãododapagliflozinpromoveaexcreçãodependente da dosedemagnésioaté1900daglicoseduranteuns24períodosdeh, comefeitoamaximalem3mg/kg. Em umratmodeldodiabetes, pré-tratamentocomosresultadospancreáticosdostreptozotocindatoxinanahiperglicemiaqueé reduzida55%pelaadministraçãode umaúnicadosede0,1mg/kgdodapagliflozincomparadacomoveículo. Osinibidoresarílicosdo O-glucósidoSGLT2eramprincipiantesadiantadosnaclínica, masoenlacearílicodo C-glucósidoencontradonodapagliflozinconfereresistênciaaometabolismoglucosidase-negociadoqueconduzàutilidadeclínicamelhoradarelativoaos O-glucósidoarílicos. Oenlacealteradodo hidrato de carbono-aglyconeexigiuoajusteconcomitantede umortoa umarylglucosidemeta-substituídoconseguirainibiçãoSGLT2poderoso. Dapagliflozinfoi sintetizadoemdiversasetapasatravésdareaçãode umaryllithiumcomgluconolactonepor-silylatedpara formaroenlacechavedo C-glucósido. Umareduçãoalfa-seletivadoheterósidoanuméricoresultantedeuobeta-Carylglucosidedesejado. Ometabolito(inativo)decirculaçãoprincipaléoresultadode3-O-glucuronidationdoglucosylmoiety. Dosmetabolitosdaminoria, doresultadooxidativoprincipaldaespéciedeO-dealkylationdo ethoxy-grupoedohydroxylationdapartedobiarylmethane. |
| Propriedades químicas | Sólido branco |
| Autor | Bristol-Myers Squibb (Estados Unidos) |
| Usos | Um inibidor do transportador 2 da sódio-glicose. |
| Usos | terapêutico para o diabetes mim ou II, e a hiperglicemia |
| Definição | ChEBI: A.A. - beta-D-glicose de inclusão glycosyl em que o grupo hidroxi anumérico é substituído por um grupo phenyl de 4 chloro-3- (4-ethoxybenzyl). Usado (no formo f seu monohidrato do propanediol) para melhorar o ontrol glycemic, junto com a dieta e o exercício, nos adultos com tipo - diabetes 2. |
| Marca | Forxiga |